Utilidad clínica de la imagen intravascular y la fisiología en la enfermedad arterial coronaria
Clinical Utility of Intravascular Imaging and Physiology in Coronary Artery Disease
Gary S. Mintz.
J Am Coll Cardiol. 2014;64(2):207-222 – doi:10.1016/j.jacc.2014.01.015
Comentario: Dr. Ernesto Duronto
En este artículo de revisión, el autor, Gary S. Mintz, analiza e intenta responder los interrogantes más comunes en la práctica diaria, respecto a la imagen anatómica de la lesión coronaria y la fisiología de la enfermedad coronaria, en la era de las imágenes y con la utilización de métodos modernos como el ultrasonido intravascular (IVUS) con caracterización tisular por radiofrecuencia (histología virtual), la tomografía de coherencia óptica (OCT), la espectroscopía y la reserva fraccional de flujo, entre otros.
El artículo es interesante y plantea preguntas como:
1. ¿Es una estenosis significativa?
Para responder esto el autor menciona estudios como el DEFER que muestra que es seguro diferir la intervención de lesiones con reserva fraccional de flujo (FFR) > 0.75, el FAME-I donde tratar lesiones con FFR >0.80 con stents liberadores de droga (SLD) de primera generación es perjudicial, y no tratarlas implica ahorrar costos y el FAME-II donde tratar lesiones con FFR
Menciona estudios de imágenes invasivos que se han intentado correlacionar con el FFR o estudios no invasivos. De ellos el diámetro luminar mínimo por IVUS es el que mejor ha sido estudiado. El corte más comúnmente empleado para vasos (no Tronco de CI) es de 3 mm2. El IVUS tiene un alto valor predictivo negativo pero muy bajo valor predictivo positivo, y justificar la intervención por este método lleva a un 50% de decisiones erróneas. Además no hay a la fecha estudios randomizados con IVUS similares a los comentados anteriormente realizados con FFR. Se menciona una evolución clínica similar cuando se compara IVUS con FFR pero tratando con stent un mayor número de lesiones con el primero de los métodos (72% vs.51.2%; p < 0.0001). La OCT no mejora el diagnóstico de la severidad de la lesión. Respecto a la caracterización tisular se menciona a la placa sin características de fibroateroma como asociada a menores eventos en el seguimiento a 3 años, sugiriéndose como un método alternativo, predictor de estabilidad. (Estudio PROSPECT). Respecto al tronco de la coronaria izquierda se mencionan 2 registros con IVUS y FFR. Se tomaron FFR >0.80 o IVUS con área luminar mínima (MLA) >6.0 mm2 como parámetros usados para diferir la revascularización y tratar médicamente a los pacientes, obteniéndose resultados similares a pacientes con FFR
Un estudio con IVUS con MLA
FFR y IVUS tienen limitaciones en enfermedad de tronco, pero el IVUS es el preferido en evaluación de enfermedad ostial de DA y CX.
2. ¿Cuál es la placa culpable?
La placa culpable puede evidenciarse por la presencia de trombo, consecuencia final del accidente o erosión de la misma. Sin embargo en casi un 50% de los pacientes en un estudio realizado en pacientes con IAM no había placa identificable o había más de una. El remodelado positivo de la placa, la coloración amarillenta de la misma o la presencia de trombo son los hallazgos más comunes en los síndromes isquémicos agudos, como así también el remodelado negativo en pacientes estables. El IVUS puede detectar placas rotas en 50% de los IAM con elevación de ST.
La OCT ve más claramente la ruptura de placa y la erosión endotelial, además de poder diferenciar entre trombo rojo y blanco, pero la sombra del primero puede ocultar la ruptura.
La espectroscopía indica que un núcleo lipídico >400 en un segmento de hasta 4 mm, es hallazgo habitual en placas causales de IAM con elevación de ST.
El IVUS y la OCT pueden además detectar nódulos calcificados y disecciones.
3. ¿Es una placa vulnerable?
El precursor de la placa trombosada es el fibroateroma de cápsula fina, tipo más común de placa vulnerable. Si bien el IVUS puede predecir inestabilidad (placa excéntrica, ecolucente), a la fecha el IVUS con histología virtual es el único método que mostró predecir eventos futuros en placas no culpables, en el estudio PROSPECT, donde los fibroateromas de cápsula fina con un MLA por IVUS 70% correlacionaron con mayor cantidad de eventos cardiovasculares a 3 años. Sub-estudios del PROSPECT mostraron además que son los remodelados extremos los que predicen inestabilidad.
La OCT puede detectar muchas características de la placa, como espesor de la capa fibrosa 0.4 mm en 7 meses, correlacionaba con signos de inestabilidad de la placa.
Se menciona que falta conocer si estas variables de placa que predicen eventos, son suficientes para indicar terapias distintas al tratamiento farmacológico, como la intervención. Para ello se está desarrollando el estudio PROSPECT-II.
4. ¿Hay riesgo de embolización distal, o IAM periprocedimiento durante la ATC al momento de implante del stent?
Los estudios muestran que un gran núcleo lipídico visto por OCT o espectroscopía, o la presencia de ruptura de placa por IVUS o OCT, así como el fibrateroma de cápsula fina, son los predictores de embolización distal y necrosis miocárdica al momento de la colocación del stent.
5. ¿Cómo optimizar los resultados de la colocación de stent en agudo?
Ya sea con stent metálico o liberador de drogas, los predictores por IVUS de trombosis o reestenosis son: el stent no expandido y la enfermedad o disección proximal o distal al stent.
Hay 4 metaanálisis de estudios randomizados con IVUS vs angiografía convencional que muestran reducción de la reestenosis, de la necesidad de nueva revascularización y de los eventos mayores (no muerte) con el IVUS.
Además se mencionan 4 metaanálisis con IVUS vs angiografía convencional con stents liberadores de droga, el más reciente con 26.503 pacientes, que muestran que el uso de IVUS reduce la trombosis de stent, la necesidad de nueva revascularización y la mortalidad, independientemente del número o largo de los stents usados.
En pacientes con IAM, 2 estudios cuestionan el valor del IVUS en la ATC primaria pero otro, el ADAPT-DES (Assessment of Dual Antiplatelet Therapy With Drug-Eluting Stents) sugiere que el IVUS tiene gran impacto en estos pacientes.
Sólo se menciona un estudio con OCT publicado a la fecha sugiriendo beneficio, similar a los metaanálisis con IVUS. El método tiene una resolución superior al IVUS, y mejor visualización de la aposición del stent o la presencia de disecciones, pero aún no hay a la fecha criterios de medición previa al implante o implantación óptima del stent por OCT. Tampoco se han correlacionado los hallazgos de la OCT con la predicción de eventos. Se menciona al FFR como la técnica de elección para valorar funcionalmente las lesiones de ramas encarceladas por el stent.
6. ¿Por qué ocurren la trombosis y reestenosis?
La mayoría de las causas de trombosis de stent y reestenosis pueden ser vistas por IVUS y OCT. Sin embargo, la nueva arterioesclerosis y la falta de cobertura de los struts por la neo-intima, causas de reestenosis y de trombosis respectivamente, sólo pueden ser identificadas por OCT, técnica de elección en estos casos. Sin embargo en el contexto agudo, la imagen vista por la tomografía dependerá de si extrajo material por aspiración o no.
Los estudios con OCT muestran que se produce nueva aterosclerosis más precoz y frecuentemente con SLD respecto a stent metálicos y se puede presentar como reestenosis o trombosis muy tardía, asociada a inestabilidad clínica y eventos cardiovasculares mayores.
Resumen de las Técnicas Recomendadas
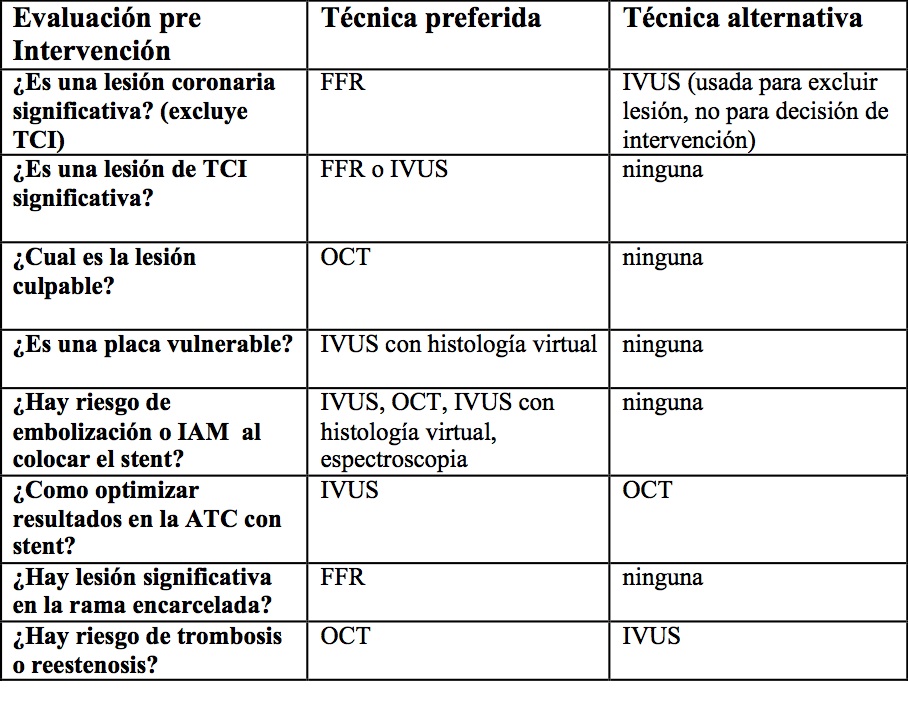
FFR: reserva fraccional de flujo. IVUS: ultrasonido intravascular. OCT: tomografía de coherencia óptica
Conclusiones finales y recomendaciones prácticas
La utilidad de estas técnicas es indiscutible a la luz de los nuevos conocimientos, con varios estudios que muestran correlación entre los hallazgos de estos métodos y el desarrollo de eventos cardiovasculares en los pacientes.
Sin embargo resta, al igual que con cualquier nuevo método de diagnóstico, conocer sus implicancias en el cambio de terapéuticas basadas en estos hallazgos. Es decir, el resultado de estos métodos diagnósticos en muchos casos, implica una evolución clínica distinta, pero ¿una terapéutica distinta a la empleada cambiará esto? Tal es el caso de la falta de evidencia actual respecto a si colocar un stent, «profilácticamente», en una placa vulnerable sin obstrucción significativa impedirá su ruptura o es suficiente un buen tratamiento con estatinas.
En nuestro medio hay 3 barreras para la implementación de estas técnicas: la económica (costos), la experiencia de los operadores y el convencimiento de los intervencionistas de las limitaciones de la angiografía sola.
La aplicabilidad masiva de ellas va a depender de sortear estas barreras. En el caso de los costos en nuestro país son todavía técnicas de disponibilidad escasa y limitadas a aprobación previa por parte de los seguros médicos, por tanto rara vez son usadas en agudo. Hay sólo algunos operadores experimentados, y otros no convencidos de su aplicabilidad.
Veremos si en el futuro, sorteadas estas barreras si se aplicarán en forma masiva, como hoy ocurre con la angiografía coronaria convencional.



